Lässt sich systemischer Lupus erythematodes (SLE) durch Hydroxychloroquin und Kortisonpräparate nicht angemessen kontrollieren, ist gemäss aktueller EULAR-Empfehlungen der Einsatz immunmodulatorischer bzw. immunsuppressiver Wirkstoffe und/oder Biologika zu prüfen. Aus Daten einer britischen Längsschnittstudie mit einem Follow-up von über 30 Jahren geht hervor, dass bestimmte Prädiktoren vorhersagen, welche Patienten von einer frühzeitigen intensivierten Therapie mit Biologika am meisten profitieren.
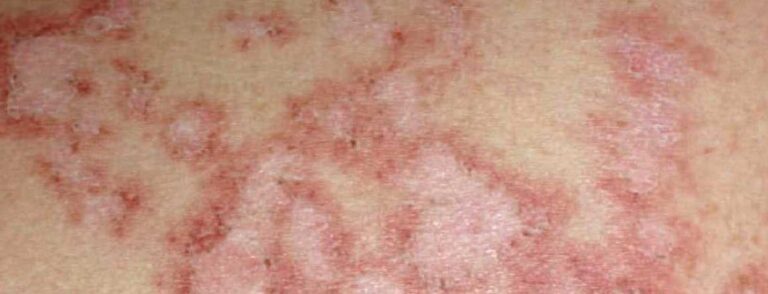
Systemischer Lupus erythematodes (SLE) ist eine chronisch-entzündliche Autoimmunerkrankung mit unterschiedlichen klinischen Manifestationen. Die Betroffenen bilden Antikörper gegen körpereigene Gewebestrukturen, sodass Autoantikörper über die Blutbahn in verschiedene Körperregionen gelangen, was zu Entzündungen an Bindegewebe, Gelenken oder Organen führen kann. Die Diagnostik orientiert sich an den EULAR/ACR-Klassifikationskriterien [1]. Typischerweise sind bei SLE antinukleäre Antikörper (ANA) und gelegentlich auch Autoantikörper gegen doppelsträngige DNA (dsDNA) zu finden. Das vorrangige Ziel in der Therapie von Patienten mit SLE besteht darin, die Krankheitsaktivität zu kontrollieren und so die Lebensqualität der Betroffenen zu verbessern. Dies soll dadurch erreicht werden, indem Entzündungsprozesse und das Auftreten bzw. die Ausprägung von Schüben reduziert werden. Welche Behandlung zum Einsatz kommt, ist unter anderem davon abhängig, welche Organe betroffen und wie häufig und stark die Schübe sind.
Was empfehlen die 2023 aufdatierten EULAR-Empfehlungen?
Die aktuellen EULAR-Guidelines zum Management von SLE heben die Wichtigkeit der folgenden vier Säulen hervor [1]:
- Frühzeitige Diagnosestellung: Trotz einer verbesserten Awareness und sensitiveren Klassifikationskriterien beträgt die mediane Diagnoselatenz gemäss neueren Studien nach wie vor 2 Jahre seit Erstmanifestation der Symptome [2–4].
- Monitoring: Insbesondere während der ersten Jahre der Erkrankung, aber auch danach ist die Überwachung auf neu auftretende Organbeteiligung ein wichtiger Faktor. Besonders wichtig ist das Erkennen von Anzeichen einer neu auftretenden Nierenbeteiligung, da Lupus-Nephritis einen wichtigen Meilenstein im natürlichen Krankheitsverlauf darstellt und eine Verzögerung der Diagnose tiefgreifende prognostische Auswirkungen hat.
- Klar definiertes Behandlungsziel: Idealerweise wird eine Remission gemäss der jüngsten DORIS(«Definition Of Remission In SLE»)-Kriterien oder alternativ eine gering ausgeprägte Krankheitsaktivität gemäss LLDAS (Lupus Low Disease Activity state) angestrebt [5]. Dies sind validierte Therapieziele, deren Erreichen nachweislich das Risiko für Schäden und andere negative Folgen der SLE implizieren [6].
- Therapieadhärenz/Compliance: Als vierte Säule wird Bedeutung der Therapietreue der Patienten betont.
Wenn sich SLE durch Hydroxychloroquin (als Monotherapie oder in Kombination mit Kortisonpräparaten) nicht dauerhaft kontrollieren lässt oder hohe Steroiddosen erforderlich sind, soll gemäss der 2023 aufdatierten EULAR-Empfehlungen die Hinzunahme von immunmodulatorischen bzw. immunsuppressiven Wirkstoffen (z.B. Methotrexat, Azathioprin oder Mycophenolat mefotil) und/oder der Biologika Belimumab oder Anifrolumab erwogen werden. Bei SLE-Patienten mit organgefährdenden oder lebensbedrohlichen Manifestationen, rät die Leitlinie dazu, intravenöses Cyclophosphamid oder in refraktären Fällen Rituximab in Betracht zu ziehen.
Längsschnittstudie zu intensivierter Therapiestrategie
Möglicherweise kann durch eine Behandlungsstrategie mit frühzeitiger Intensivtherapie schweren SLE-Verlaufsformen und akkumulativen Schäden entgegengewirkt werden, was voraussetzt, dass Risikopatienten im entsprechenden Zeitfenster identifiziert werden. Gemäss Dr. Porntip Intapiboon von der University of Leeds (UK) gebe es grundsätzlich zwei Gruppen von SLE-Patienten, die von einer intensivierten Therapiestrategie mit Biologika oder Cyclophosphamid profitieren können [7]:
- Patienten, die zum Zeitpunkt der Diagnose eine schwere SLE aufweisen,
- Patienten mit einer milden Form von SLE, welche auf konventionelle Behandlung (s.o.) ein mangelhaftes Ansprechen zeigt.
Ob es bezüglich Krankheitsaktivität und Komplementspiegel konkrete Cut-off Werte gibt, an denen man sich für die Therapiesteuerung orientieren kann, ist bislang nicht geklärt. Um Näheres darüber herauszufinden, haben Intapiboon et al. eine retrospektive Analyse durchgeführt, in welche alle Patienten mit einer SLE-Diagnose aus zwei «Leeds SLE Inception Cohort»-Datenbanken mit einem Follow-up von über 30 Jahren inkludiert wurden [7].
Insgesamt wurden 229 SLE-Patienten eingeschlossen, davon waren 91,3% weiblich; das mittlere Alter bei der SLE-Diagnose betrug 38,8 (SD14,7) Jahre (Abb. 1) [7]. Bei 48,1% (n=110) der Patienten wurde eine Intensivtherapie eingeleitet; bei 17,0% (n=39) innerhalb eines Jahres und bei 24,0% (n=55) innerhalb von zwei Jahren nach der Diagnose. Der Median der Zeit von der SLE-Diagnose bis zum Beginn der Intensivtherapie betrug 2 Jahre (IQR 0,5–8).
Univariate Analysen ergaben, dass während der ersten zwei Jahre nach der SLE-Diagnose positive anti-Ro-Antikörper (SS-A), niedrige Komplementspiegel, ein Score ≥20 gemäss EULAR-ACR-Kriterien und ein höherer Score im Systemic Lupus Erythematosus Disease Activity Index-2K (SLEDAI) mit einer erhöhten Wahrscheinlichkeit für eine intensivierte Therapie assoziiert waren. In der ROC-Analyse wurde ein SLEDAI-Score von ≥9 als relevanter Cut-off-Wert ermittelt. Und aus der multivariaten Analyse ging hervor, dass niedrige Komplementspiegel und ein SLEDAI-Score von ≥9 mit einer erhöhten Wahrscheinlichkeit für eine intensivierte Therapie einhergingen (Tab. 1). Die Frage der Therapiesequenz bei SLE sei aktuell nicht eindeutig geklärt, so Dr. Intapiboon. Die Ergebnisse der vorliegenden Studie weisen darauf hin, dass Patienten, bei welchen die identifizierten Prädiktoren gegeben sind, ein höheres Risiko haben, zum einen eine schwerere Form von SLE entwickeln und zum anderen auf konventionelle Therapien mangelhaft anzusprechen. Diese Subgruppen von SLE-Patienten profitieren möglicherweise von einer Erstlinien-Therapie mit Biologika, so ein Fazit der Studie.
Kongress: EULAR Annual Meeting
Literatur:
- Fanouriakis A, et al.: EULAR recommendations for the management of systemic lupus erythematosus: 2023 update. Ann Rheum Dis 2024; 83(1): 15–29.
- Aringer M, et al.: European league against rheumatism/American college of rheumatology classification criteria for systemic lupus erythematosus. Ann Rheum Dis 2019; 78: 1151–1159.
- Kapsala NN, et al.: From first symptoms to diagnosis of systemic lupus erythematosus: mapping the journey of patients in an observational study. Clin Exp Rheumatol 2023; 41: 74–81.
- Kernder A, et al.: Delayed diagnosis adversely affects outcome in systemic lupus erythematosus: cross sectional analysis of the lula cohort. Lupus 2021; 30: 431–438.
- van Vollenhoven RF, et al.: DORIS definition of remission in SLE: final recommendations from an international task force. Lupus Sci Med 2021; 8: e000538.
- Franklyn K, et al.: Definition and initial validation of a lupus low disease activity state (LLDAS). Ann Rheum Dis 2016;75: 1615–1621.
- Intapiboon P, et al.: identifying a population of patients for intensive first-line therapy in SLE: a clinical and biomarker model to predict the need for intensive therapy, OP0187, EULAR Annual Meeting, Vienna, 12–15 june, 2024.
AUTOR: Mirjam Peter, M.Sc.